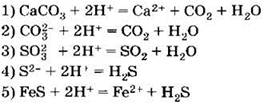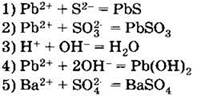Химия 11 класс - контрольные и проверочные работы к учебнику О. С. Габриелян - 2016 год
Электролитическая диссоциация
ВАРИАНТ 1
Часть А. Тестовые задания с выбором одного правильного ответа
А1. Электрическая лампочка загорится при опускании электродов в
1) водный раствор этилового спирта
2) безводную серную кислоту
3) водный раствор ацетата калия
4) водный раствор сахарозы
А2. Сильным электролитом является
1) H2SO3 .
2) HF .
3) K2SO3
4) C6H5NH3OH
А3. Наибольшее количество ионов водорода содержится в 100 мл 0,1 М раствора
1) НСООН .
2) С2Н5СООН
3) С3Н7СООН
4) С4Н8СООН
А4. Ступенчатая диссоциация возможна в растворе
1) HNO3 .
2) KAl(SO4)2 .
3) FeCl3
4) NaH2PO4
A5. Какие из утверждений о процессе диссоциации верны?
А. Степень диссоциации уксусной кислоты возрастает при разбавлении раствора.
Б. Нагревание подавляет процесс диссоциации фтороводородной кислоты в водном растворе.
1) верно только .
2) верно только .
3) верны оба суждения
4) неверны оба суждения
А6. Одновременно в растворе не могут находиться ионы
![]()
А7. Газ выделяется при взаимодействии разбавленной серной кислоты с растворами обоих веществ в группе
![]()
А8. Как бромид калия, так и фосфат натрия образуют осадок при взаимодействии с раствором
1) СаСl2
2) AgNO3
3) CuSO4
4) Ba(NO3)2
А9. Сокращённое ионное уравнение
![]()
соответствует взаимодействию между веществами
![]()
А10. В таблице представлены значения произведения растворимости (ПР) солей серебра.
|
Формула соли |
AgCl |
AgBr |
AgI |
AgSCN |
|
ПР |
1,8 ∙ 10-10 |
5,4 ∙ 10-13 |
8,5 ∙ 10-17 |
1,0 ∙ 10-12 |
Наибольшая концентрация (моль/л) ионов Ag+ существует в насыщенном растворе
1) AgCl
2) AgBr .
3) Agl .
4) AgSCN
Часть В. Тестовые задания с выбором трёх правильных ответов (В1) и на соответствие (В2 и В3)
В1. Сокращённое ионное уравнение
![]()
соответствует процессам взаимодействия между
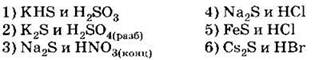
В2. Установите соответствие между реагентами и кратким ионным уравнением их взаимодействия.
|
РЕАГЕНТЫ A) сульфит калия и соляная кислота Б) карбонат калия и азотная кислота B) карбонат кальция и соляная кислота Г) сульфид железа (II) и соляная кислота |
КРАТКОЕ ИОННОЕ УРАВНЕНИЕ
|
В3. Установите соответствие между значением pH и средой водного раствора.
|
ЗНАЧЕНИЕ pH |
СРЕДА РАСТВОРА |
|
А) 8,9 |
1) кислотная |
|
Б) 3,2 |
2) нейтральная |
|
В) 7,0 |
3) щелочная |
|
Г) 14,0 |
Часть С. Задания с развёрнутым ответом
С1. Определите pH раствора бромоводородной кислоты, концентрация НВr в котором равна 0,01 моль/л. Степень диссоциации кислоты принять равной 100%.
С2. Определите растворимость (моль/л) сульфата свинца в воде. Произведение растворимости сульфата свинца равно 1,6 ∙ 10-8.
ВАРИАНТ 2
Часть А. Тестовые задания с выбором одного правильного ответа
А1. Электрическая лампочка загорится при опускании электродов в
1) водный раствор глюкозы
2) расплав хлорида калия
3) раствор фенола в бензоле
4) расплав сахарозы
А2. Наиболее слабым электролитом является
1) Н2.
2) H2.
3) H2Se
4) Н2Те
А3. Наибольшее количество ионов водорода содержится в 100 мл 0,1М раствора
![]()
А4. Ступенчатая диссоциация возможна в растворе
1) азотной кислот.
2) сульфата натри.
3) хлорида хрома (II)
4) гидросульфита натрия
А5. Какие из утверждений о процессе диссоциации верны?
А. Степень диссоциации муравьиной кислоты не зависит от концентрации раствора.
Б. Понижение температуры подавляет процесс диссоциации азотистой кислоты в водном растворе.
1) верно только .
2) верно только .
3) верны оба суждения
4) неверны оба суждения
А6. Одновременно в растворе не могут находиться ионы
![]()
А7. Газ выделяется при взаимодействии соляной кислоты с растворами обоих веществ
![]()
А8. Как хлорид меди (II), так и сульфат железа (II) образуют осадок при взаимодействии с раствором
![]()
A9. Сокращённое ионное уравнение Н+ + ОН- = Н2O соответствует взаимодействию между веществами
![]()
А10. В таблице представлены значения произведения растворимости (ПР) солей бария.
|
Формула соли |
ВаСO3 |
BaSeO4 |
ВаМоO4 |
BaSO4 |
|
ПР |
2,6 ∙ 10-9 |
3,4 ∙ 10-8 |
3,5 ∙ 10-8 |
1,1 ∙ 10-10 |
Наибольшая полнота осаждения ионов Ва2+ из раствора ВаСl2 достигается добавлением раствора
![]()
Часть В. Тестовые задания с выбором трёх правильных ответов (В1) и на соответствие (В2 и В3)
В1. Сокращённое ионное уравнение
![]()
соответствует процессам взаимодействия между
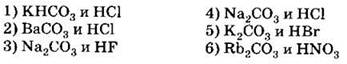
В2. Установите соответствие между реагентами и кратким ионным уравнением их взаимодействия.
|
РЕАГЕНТЫ A) гидроксид натрия и серная кислота Б) гидроксид бария и соляная кислота B) нитрат свинца (II) и сульфид калия Г) нитрат свинца (II) и гидроксид калия |
КРАТКОЕ ИОННОЕ УРАВНЕНИЕ
|
В3. Установите соответствие между значением pH и средой водного раствора.
|
ЗНАЧЕНИЕ pH A) 10,0 Б) 7,0 B) 2,5 Г) 4,1 |
СРЕДА РАСТВОРА 1) кислотная 2) нейтральная 3) щелочная |
Часть С. Задания с развёрнутым ответом
С1. Определите pH раствора гидроксида калия, концентрация КОН в котором равна 0,001 моль/л. Степень диссоциации гидроксида калия принять равной 100%.
С2. Определите, выпадет ли осадок хлорида серебра, если смешать равные объёмы растворов хлорида натрия и нитрата серебра, концентрации которых соответственно равны 1 ∙ 10-5 моль/л и 2 ∙ 10-5 моль/л. Произведение растворимости хлорида серебра составляет 1,77 ∙ 10-10.