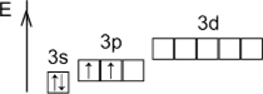Химия 9 класс - поурочные разработки
Кремний и его соединения. Стекло. Цемент
Цели урока: знать состав, строение, свойства оксидов кремния; уметь сравнивать состав и строение оксидов кремния; уметь доказывать химические свойства оксида кремния, записывать уравнения реакций в молекулярном, ионном и сокращенном ионном виде.
Ход урока
1. Организационный момент урока.
2. Изучение нового материала.
КРЕМНИЙ
Открыт Ж. Гей-Люссаком и Л. Тенаром в 1811г.
Второй по распространённости элемент в земной коре после кислорода (27,6% по массе). Встречается в соединениях.
Строение атома кремния в основном состоянии
1s22s22p63s23p2
|
Строение атома кремния в возбуждённом состоянии 1s22s22p63s13p3
Степени окисления: +4, -4. |
Аллотропия кремния
Известен аморфный и кристаллический кремний.
Поликристаллический кремний
Кристаллический – тёмно-серое вещество с металлическим блеском, большая твёрдость, хрупок, полупроводник; ρ = 2,33 г/см3, t°пл. = 1415 °C; t°кип. = 2680 °C.
Имеет алмазоподобную структуру и образует прочные ковалентные связи. Инертен.
Аморфный - бурый порошок, гигроскопичен, алмазоподобная структура, ρ = 2 г/см3, более реакционноспособен.
Получение кремния
1) Промышленность – нагревание угля с песком:
2C + SiO2 t˚→ Si + 2CO
2) Лаборатория – нагревание песка с магнием:
2Mg + SiO2 t˚→ Si + 2MgO Опыт
Химические свойства
Типичный неметалл, инертен.
Как восстановитель:
1) С кислородом
Si0 + O2 t˚→ Si+4O2
2) С фтором (без нагревания)
Si0 + 2F2 → SiF4
3) С углеродом
Si0 + C t˚→ Si+4C
(SiC - карборунд - твёрдый; используется для точки и шлифовки)
4) С водородом не взаимодействует.
Силан (SiH4) получают разложением силицидов металлов кислотой:
Mg2Si + 2H2SO4 → SiH4 + 2MgSO4
5) С кислотами не реагирует (только с плавиковой кислотой Si+4HF = SiF4 + 2H2)
Растворяется только в смеси азотной и плавиковой кислот:
3Si + 4HNO3 + 18HF → 3H2[SiF6] + 4NO + 8H2O
6) Со щелочами (при нагревании):
Si0 + 2NaOH + H2O t˚→ Na2Si+4O3+ 2H2
Как окислитель:
7) С металлами (образуются силициды):
Si0 + 2Mg t˚→ Mg2Si-4
Применение кремния
Кремний широко используется в электронике как полупроводник. Добавки кремния к сплавам повышают их коррозионную стойкость. Силикаты, алюмосиликаты и кремнезем – основное сырье для производства стекла и керамики, а также для строительной промышленности.
Силан - SiH4
Физические свойства: Бесцветный газ, ядовит, t°пл. = -185 °C, t°кип. = -112 °C.
Получение: Mg2Si + 4HCl → 2MgCl2 + SiH4↑
Химические свойства:
1) Окисление: SiH4 + 2O2 t˚→ SiO2 + 2H2O
2) Разложение: SiH4 → Si + 2H2
Оксид кремния (IV) - (SiO2)n
SiO2 - кварц, горный хрусталь, аметист, агат, яшма, опал, кремнезём (основная часть песка):
Кристаллическая решётка оксида кремния (IV) – атомная и имеет такое строение:
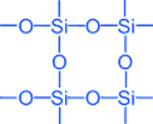
Al2O3 · 2SiO2 · 2H2O - каолинит (основная часть глины)

K2O · Al2O3 · 6SiO2 - ортоклаз (полевой шпат)

Физические свойства: Твёрдое, кристаллическое, тугоплавкое вещество, t°пл. = 1728 °C, t°кип. = 2590 °C.
Химические свойства:
Кислотный оксид. При сплавлении взаимодействует с основными оксидами, щелочами, а также с карбонатами щелочных и щелочноземельных металлов:
Изучение свойств оксида кремния (IV)
1) С основными оксидами:
SiO2 + CaO t˚→ CaSiO3
2) Со щелочами:
SiO2 + 2NaOH t˚→ Na2SiO3 + H2O
3) С водой не реагирует
4) С солями:
SiO2 + CaCO3 t˚→ CaSiO3 + CO2
SiO2 + K2CO3 t˚→ K2SiO3 + CO2
5) С плавиковой кислотой:
SiO2 + 4HF t˚→ SiF4 + 2H2O
SiO2 + 6HF t˚→ H2[SiF6] (гексафторкремниевая кислота) + 2H2O
(реакции лежат в основе процесса травления стекла).
Применение:
1. Изготовление силикатного кирпича
2. Изготовление керамических изделий
3. Получение стекла
Кремниевые кислоты
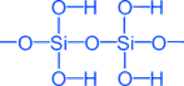
x · SiO2 · y H2O
x = 1, y = 1 H2SiO3 - метакремниевая кислота
x = 1, y = 2 H4SiO4 - ортокремниевая кислота и т. д.
Физические свойства: H2SiO3 - очень слабая (слабее угольной), непрочная, в воде малорастворима (образует коллоидный раствор), не имеет кислого вкуса.
Получение:
Действие сильных кислот на силикаты - Na2SiO3 + 2HCl → 2NaCl + H2SiO3↓
Химические свойства:
При нагревании разлагается: H2SiO3 t˚→ H2O + SiO2
Соли кремниевой кислоты - силикаты.
1) с кислотами
Na2SiO3 + H2O + CO2 = Na2CO3 + H2SiO3
Качественная реакция на силикаты.
В пробирку с раствором силикати калия добавили раствор разбавленной соляной кислоты.
В пробирке образовалась белая полутвердая масса – кремниевая кислота (H2SiO3)
![]()
2) с солями
Na2SiO3 + CaCl2 = 2NaCl + CaSiO3↓
3) Силикаты, входящие в состав минералов, в природных условиях разрушаются под действием воды и оксида углерода (IV) - выветривание горных пород:
(K2O · Al2O3 · 6SiO2) (полевой шпат) + CO2 + 2H2O → (Al2O3 · 2SiO2 · 2H2O)(каолинит (глина)) + 4SiO2(кремнезём (песок)) + K2CO3
Применение соединений кремния
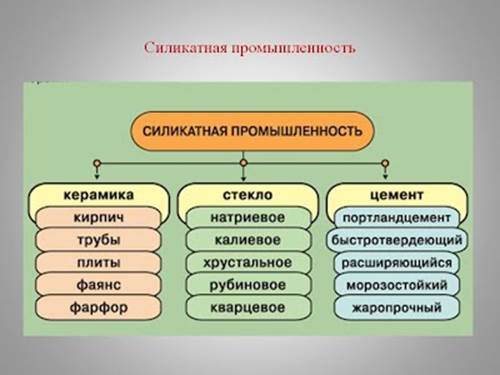
Природные соединения кремния - песок (SiO2) и силикаты используются для производства керамики, стекла и цемента.
Керамика.
Сырье: глина, песок, минеральные добавки.
Стадии производства:
Керамическая масса → формирование → сушка → обжиг → покрытие глазурью.
Обжиг:
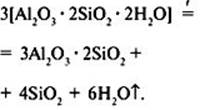
Продукция: кирпич, канализационные и дренажные трубы, облицовочные плиты, фаянс, фарфор.
Керамика |
|
Фарфор = каолин + глина + кварц + полевой шпат. Родина фарфора – Китай, где фарфор известен уже в 220 г. В 1746 г – налажено производство фарфора в России
|
Фаянс - от названия итальянского города Фаэнца. Где в 14-15 веках было развито керамическое ремесленничество. Фаянс – отличается от фарфора большим содержанием глины (85%), более низкой температурой обжига.
|
Стекло – хрупкий, прозрачный материал, способен размягчаться и при застывании принимает любую форму. Стекло получают варкой шихты (сырьевой смеси, состоящей из песка, соды и известняка) в специальных стекловаренных печах.
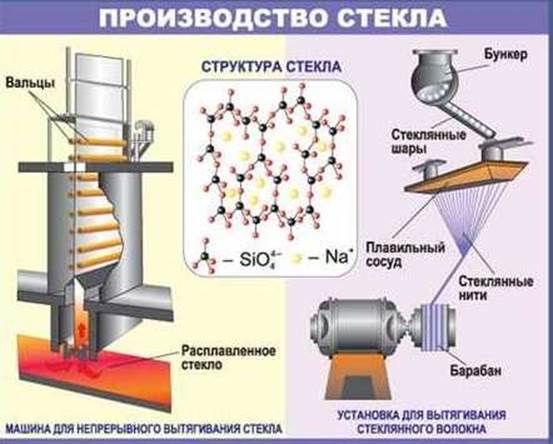
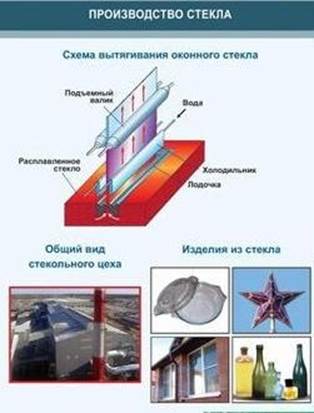
Основные реакции, протекающие при плавке шихты
1. Na2CO3 + SiO2 = Na2SiO3 + CO2
2. CaCO3 + SiO2 = CaSiO3 + CO2
3. Na2SiO3 + CaSiO3 + 4SiO2 = Na2O · CaO · 6SiO2 - формула оконного стекла
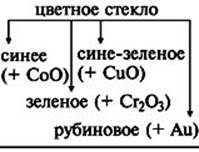
При добавлении оксида свинца получают хрусталь.
Стекло.
Сырье: кварцевый песок, известняк.
Варка стекла:
Стекло оконное:
Na2O · CaO · 6SiO2,
тугоплавкое:
К2O · CaO · 6SiO2,
хрустальное:
Na2O · PbO · 6SiO2
Цемент

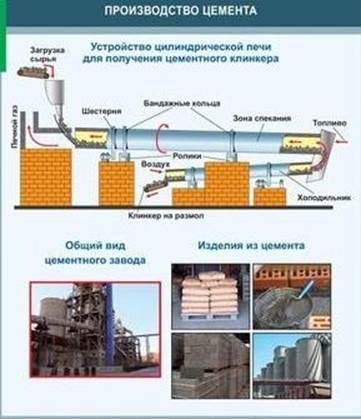
Цемент – мелко измельчённый клинкер с минеральными добавками.
Клинкер - шарики тёмно-серого цвета получают спеканием глины и известняка в специальных вращающихся печах
3. Закрепление изученного материала
Осуществите превращения по схеме:
1) Si → SiO2 → Na2SiO3 → H2SiO3 →SiO2
2) Si → Mg2Si → SiH4 → SiO2
3) Si → Na2SiO3
4. Домашнее задание
П. 30-33, упр. 1, 3-5, 8, 9 на стр. 101.