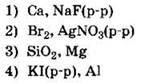Химия 9 класс - Основной государственный экзамен - Типовые тестовые задания А. С. Корощенко - 2018 год
ВАРИАНТ 1 - ВАРИАНТЫ ЭКЗАМЕНАЦИОННОЙ РАБОТЫ
Часть 1
При выполнении заданий 1-15 в поле ответа запишите одну цифру, которая соответствует номеру правильного ответа.
1. Химическому элементу, в атоме которого распределение электронов по слоям ![]() соответствует символ этого элемента, формула высшего оксида и водородного соединения:
соответствует символ этого элемента, формула высшего оксида и водородного соединения:
![]()
[ ]
2. В каком ряду элементы расположены в порядке уменьшения их электроотрицательности?
1) азот — углерод — бор
2) кремний — фосфор — сера
3) германий — кремний — углерод
4) фтор — бром — хлор
[ ]
3. Соединениями с ковалентной неполярной и ионной связью являются соответственно
1) оксид фосфора(V) и оксид натрия
2) хлорид натрия и хлор
3) азот и сульфид натрия
4) хлорид кальция и хлороводород
[ ]
4. Максимально возможную степень окисления атом серы проявляет в соединении
![]()
[ ]
5. Сложным является каждое из двух веществ:
1) вода и хлор
2) вода и водород
3) водород и кварц
4) этанол и вода
[ ]
6. Если прокалить кусочек мела, дать ему остыть, а затем поместить в пробирку с небольшим количеством воды, в которую добавлено несколько капель фенолфталеина, то:
1) не произойдет никаких изменений
2) окраска содержимого пробирки станет малиновой
3) образуется прозрачный бесцветный раствор
4) наблюдается выделение пузырьков газа
[ ]
7. Сульфит-ионы образуются при электролитической диссоциации
![]()
[ ]
8. Краткое ионное уравнение Н+ + ОН- = Н2O отвечает взаимодействию веществ:

[ ]
9. Не взаимодействуют между собой вещества, формулы которых:

[ ]
10. Две соли образуются при растворении в соляной кислоте оксида
![]()
[ ]
11. Гидроксид железа(II) реагирует с раствором
1) сульфата натрия
2) карбоната калия
3) хлорида кальция
4) бромоводорода
[ ]
12. Соль не образуется в ходе реакции
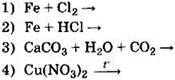
[ ]
13. Верны ли следующие суждения о правилах безопасной работы в химической лаборатории?
А. Полученный из пероксида водорода кислород нельзя определять по запаху.
Б. Водород, полученный в результате взаимодействия цинка с соляной кислотой, при поджигании не надо проверять на чистоту.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
[ ]
14. В уравнении окислительно-восстановительной реакции
![]()
коэффициент перед формулой восстановителя равен
1) 4
2) 3
3) 2
4) 1
[ ]
15. На какой диаграмме распределение массовых долей элементов соответствует количественному составу сульфата аммония:

[ ]
При выполнении заданий 16, 17 из предложенного перечня ответов выберите два правильных и запишите в таблицу цифры, под которыми они указаны.
16. Общим для серы и хлора является
1) одинаковое значение электроотрицательности
2) образование ими высших оксидов с общей формулой ЭO3
3) наличие трех электронных слоев в их атомах
4) одинаковое число электронов на внешнем электронном слое
5) способность взаимодействовать с большинством металлов
Ответ: ![]()
17. Уксусная кислота не вступает во взаимодействие с
1) оксидом углерода(IV)
2) оксидом кальция
3) медью
4) гидроксидом натрия
5) карбонатом калия
Ответ: ![]()
При выполнении заданий 18, 19 к каждому элементу первого столбца подберите соответствующий элемент из второго столбца. Запишите в таблицу выбранные цифры под соответствующими буквами. Цифры в ответе могут повторяться.
18. Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества. К каждому элементу первого столбца подберите соответствующий элемент из второго столбца.
|
ВЕЩЕСТВА |
РЕАКТИВ |
||||
|
|
|
||||
|
А |
Б |
В |
|||
19. Установите соответствие между названием вещества и реагентами, с которыми это вещество может взаимодействовать.
|
НАЗВАНИЕ ВЕЩЕСТВА |
РЕАГЕНТЫ |
||||
|
А) бром |
|
||||
|
Б) плавиковая кислота |
|||||
|
В) иодид натрия |
|||||
|
А |
Б |
В |
|||
Часть 2
Для ответов на задания 20-22 используйте отдельный лист. Запишите сначала номер задания (20, 21, 22), а затем развернутый ответ к нему. Ответы записывайте четко и разборчиво.
20. Используя метод электронного баланса, составьте уравнение реакции
![]()
Определите окислитель и восстановитель.
21. При растворении 180 г известняка в избытке азотной кислоты выделилось 34,27 л (н.у.) углекислого газа. Определите массовую долю карбоната кальция в данном образце известняка.
22. Даны вещества: Fe, НСl(разб.), Сu, К3РO4, NaOH, (СuOН)2СO3. Используя воду и необходимые вещества только из этого списка, получите в две стадии гидроксид меди(II). Опишите признаки проводимых реакций. Для первой реакции напишите сокращенное ионное уравнение.