Физика - Поурочные планы к учебникам Г. Я. Мякишева, С. В. Громова и В. Л. Касьянова 10 класс
Распределение молекул идеального газа в пространстве - МОЛЕКУЛЯРНО-КИНЕТИЧЕСКАЯ ТЕОРИЯ
Цель: сформировать понятия: макроскопические, микроскопические параметры, статистическая закономерность.
Ход урока
I. Повторение изученного
1. Назовите основные агрегатные состояния вещества?
2. Какие изменения происходят в веществе при фазовых переходах?
3. При каком условии вещество находится в твердом состоянии?
4. Как движутся молекулы в твердом теле?
5. При каком условии образуется жидкое состояние вещества?
6. В чем особенности движения молекул в жидкости?
7. При каком условии вещество находится в газообразном состоянии?
8. Назовите состав трехкомпонентной плазмы.
II. Лабораторная работа «Наблюдение взаимодействия различных веществ»
Цель работы: убедиться в существовании взаимодействия частиц вещества
Приборы и материалы: кусок пластилина; две парафиновые свечи; спички; два предметных стекла, стакан с водой; пипетка; ластик.
Ход работы
1. Разделите кусок пластилина на две одинаковые части, а затем прижмите их друг к другу. Что вы наблюдаете?
2. Приведите в соприкосновение две парафиновые свечи. Соединились они или нет? Почему?
3. Оплавьте конец одной свечи на пламени спички. Соедините свечи. Что вы наблюдаете? Почему?
4. Сложите два сухих предметных стекла. Прижмите их друг к другу. Что вы наблюдаете?
5. С помощью пипетки наберите воду из стакана. Смочите дно из стекол водой (капните из пипетки несколько капель) и опять прижмите предметные стекла друг к другу. Что вы наблюдаете? Почему?
6. Сожмите пальцами ластик. Что вы ощущаете? Почему ластик восстанавливает свою первоначальную форму после прекращения сжатия?
III. Изучение нового материала
К системе с очень большим числом частиц законы механики непосредственно применять невозможно. Место механики занимает статистическая механика. Она позволяет вычислить средние значения физических величин, которые регистрируются макроскопическими приборами.
Свойства и состояние макроскопического тела определяются характером взаимодействия и движения слагающих его частиц. Значение любого термодинамического параметра связано с движением молекул или атомов тела. Механика Ньютона хорошо приспособлена для описания движения небольшого числа тел. Если же число движущихся частиц достигает миллионов, то чисто механический подход теряет смысл. В этой ситуации не помогут никакие вычислительные машины. Однако задача исследования систем из огромного числа частиц все же поддается решению, в поведении таких систем обнаруживается определенные закономерности. Но это уже другие закономерности, закономерности нового типа статистической физики. Важно знать не поведение отдельных молекул, а средний результат, к которому приводит их совокупное движение. Этот результат находят с помощью законов статистической физики.
С течением времени микросостояния непрерывно сменяют друг друга. Время пребывания системы в определенном макроскопическом состоянии пропорционально числу микросостоянийZ1, которые реализуют данное состояние. Если через Z обозначить полное число микросостояний системы, то вероятность W определяется ![]()
Чем больше Z, тем больше вероятность данного макросостояния и тем большее время система будет находиться в этом состоянии. Эволюция системы происходит в направлении перехода от маловероятных состояний к состояниям более вероятным. Именно с этим связана необратимость течения макроскопических процессов. Обратный процесс не является невозможным, он просто маловероятен.
IV. Самостоятельная работа
(Смотри раздел «Самостоятельные и контрольные работы».)
Ответы:
Вариант 1: 1. 15 · 1022. 2. 2,2 кг. 3. 7 · 10-3 кг. 4. 18 · 1026. 5. ≈ 1020
Вариант 2: 1. ≈ 5,3 · 10-26. 2. 200 моль. 3. 0,52 кг. 4. mPb > mSn в 1,7 раза. 5. NAl ≈ NAg
V. Кроссворд «Строение вещества»
Вариант 1
1. Рассчитайте число молекул, содержащихся в 1 г гелия.
2. Какова масса 50 молей углекислого газа?
3. Рассчитайте массу 2 · 1023 молекул азота.
4. Сколько молекул содержится в 5 м3 олова? Плотность олова 7300 кг/м3.
5. На изделие, поверхность которого 20 см2, нанесли слой серебра толщиной 1 мкм. Сколько атомов серебра содержится в покрытии? Плотность серебра 10,5 · 103 кг/м3.
Вариант 2
1. Рассчитайте массу молекулы кислорода.
2. Какое количество вещества содержится в алюминиевой отливке массой 5,4 кг?
3. Какова масса 20 молей ацетона С2Н2?
4. Сравните массы тел, сделанных из олова и свинца, если они содержат равные количества вещества.
5. Сравните число атомов, из которых состоят серебряная и алюминиевая ложки равного объема. Плотность серебра 10,5 · 103 кг/м3, а алюминия - 2,7 · 103 кг/м3.
Кроссворд «Строение вещества»
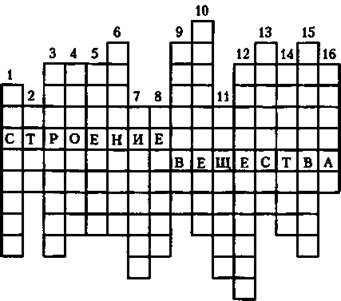
1. Газ, без которого невозможна жизнь человека. 2. Химически неделимая часть молекулы. 3. Оптический прибор для получения изображений неразличимых невооруженным глазом предметов. 4. Древнегреческий ученый. 5. Наименьшая частица вещества, обладающая его химическими свойствами. 6. Великий русский ученый, один из основателей учения о молекулярном строении вещества. 7. Явление проникновения молекул одного вещества в промежутки между молекулами другого вещества. 8. Шведский ученый, в честь которого названа температурная шкала. 9. Общее название физических явлений нагревания, охлаждения, таяния, плавления, кипения. 10. Явление взаимного тяготения тел. 11.... - это то, из чего состоит однородное физическое тело. 12. Чем больше средняя скорость молекул тела, тем выше его... 13. Одно из агрегатных состояний вещества. 14. Научное предположение. 15. Физическое явление на границе соприкосновения твердого тела, жидкости и газа. 16. Морская птица, способная глубоко нырять.
Ответы: 1. Кислород. 2. Атом. 3. Микроскоп. 4. Демокрит. 5. Молекула. 6. Ломоносов. 7. Диффузия. 8. Цельсий. 9. Тепловые. 10. Притяжение. 11. Вещество. 12. Температура. 13. Жидкость. 14. Гипотеза. 15. Смачивание. 16. Баклан.
Домашнее задание
Прочитать конспект в тетради. С. 159 (3-4).