Физика: Универсальный справочник
Состав ядра - Физика атомного ядра - ОСНОВЫ СПЕЦИАЛЬНОЙ ТЕОРИИ ОТНОСИТЕЛЬНОСТИ. КВАНТОВАЯ ФИЗИКА
4.8. Физика атомного ядра
4.8.1. Состав ядра
Атомное ядро — это центральная часть атома, состоящая из протонов и нейтронов (которые вместе называются нуклонами).
Ядро было открыто Э. Резерфордом в 1911 г. при исследовании прохождения а-частиц через вещество. Оказалось, что почти вся масса атома (99,95%) сосредоточена в ядре. Размер атомного ядра имеет порядок величины 10 -13-10 -12 см, что в 10 000 раз меньше размера электронной оболочки.
Предложенная Э. Резерфордом планетарная модель атома и экспериментальное наблюдение им ядер водорода, выбитых а-частицами из ядер других элементов (1919-1920 гг.), привели ученого к представлению о протоне. Термин протон был введен в начале 20-х гг. XX ст.
Протон (от греч. protos — первый, символ р) — стабильная элементарная частица, ядро атома водорода.
Протон — положительно заряженная частица, заряд которой по абсолютной величине равен заряду электрона е = 1,6 · 10-19 Кл. Масса протона в 1836 раз больше массы электрона. Масса покоя протона mр = 1,6726231 · 10 -27 кг = 1,007276470 а.е.м.
Второй частицей, входящей в состав ядра, является нейтрон. Нейтрон (от лат. neuter — ни тот, ни другой, символ n) — это элементарная частица, не имеющая заряда, т. е. нейтральная.
Масса нейтрона в 1839 раз превышает массу электрона. Масса нейтрона почти равна (незначительно больше) массе протона: масса покоя свободного нейтрона mп = 1,6749286 х 10 -27 кг = 1,0008664902 а.е.м. и превосходит массу протона на 2,5 массы электрона. Нейтрон, наряду с протоном под общим названием нуклон входит в состав атомных ядер.
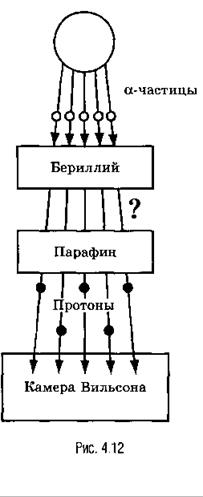
Нейтрон был открыт в 1932 г. учеником Э. Резерфорда Д. Чедвигом при бомбардировке бериллия α-частицами. Возникающее при этом излучение с большой проникающей способностью (преодолевало преграду из свинцовой пластины толщиной 10-20 см) усиливало свое действие при прохождении через парафиновую пластину (рис. 4.12). Оценка энергии этих частиц по трекам в камере Вильсона, сделанная супругами Жолио-Кюри, и дополнительные наблюдения позволили исключить первоначальное предположение о том, что это ɣ-кванты. Большая проникающая способность новых частиц, названных нейтронами, объяснялась их электронейтральностью. Ведь заряженные частицы активно взаимодействуют с веществом и быстро теряют свою энергию.
Существование нейтронов было предсказано Э. Резерфордом за 10 лет до опытов Д. Чедвига. При попадании а-частиц в ядра бериллия происходит следующая реакция:
![]()
Здесь ![]() — символ нейтрона; заряд его равен нулю, а относительная атомная масса приблизительно равна единице. Нейтрон — нестабильная частица: свободный нейтрон за время ~15 мин. распадается на протон, электрон и нейтрино — частицу, лишенную массы покоя.
— символ нейтрона; заряд его равен нулю, а относительная атомная масса приблизительно равна единице. Нейтрон — нестабильная частица: свободный нейтрон за время ~15 мин. распадается на протон, электрон и нейтрино — частицу, лишенную массы покоя.
После открытия Дж. Чедвиком нейтрона в 1932 г. Д. Иваненко и В. Гейзенберг независимо друг от друга предложили протонно-нейтронную (нуклонную) модель ядра. Согласно этой модели, ядро состоит из протонов и нейтронов. Число протонов Z совпадает с порядковым номером элемента в таблице Д. И. Менделеева.
Заряд ядра Q определяется числом протонов Z, входящих в состав ядра, и кратен абсолютной величине заряда электрона е:
![]()
Число Z называется зарядовым числом ядра или атомным номером.
Массовым числом ядра А называется общее число нуклонов, т. е. протонов и нейтронов, содержащихся в нем. Число нейтронов в ядре обозначается буквой N. Таким образом, массовое число равно:
![]()
Нуклонам (протону и нейтрону) приписывается массовое число, равное единице, электрону — нулевое значение.
Представлению о составе ядра содействовало также открытие изотопов.
Изотопы (от греч. isos — равный, одинаковый и topos — место) — это разновидности атомов одного и того же химического элемента, атомные ядра которых имеют одинаковое число протонов (Z) и различное число нейтронов (N).
Изотопами называются также ядра таких атомов. Изотопы являются нуклидами одного элемента. Нуклид (от лат. nucleus — ядро) — любое атомное ядро (соответственно атом) с заданными числами Z и N. Общее обозначение нуклидов имеет вид![]() , где X — символ химического элемента, A = Z + N — массовое число.
, где X — символ химического элемента, A = Z + N — массовое число.
Изотопы занимают одно и то же место в Периодической системе элементов, откуда и произошло их название. По своим ядерным свойствам (например, по способности вступать в ядерные реакции) изотопы, как правило, существенно отличаются. Химические (и почти в той же мере физические) свойства изотопов одинаковы. Это объясняется тем, что химические свойства элемента определяются зарядом ядра, поскольку именно он влияет на структуру электронной оболочки атома.
Исключением являются изотопы легких элементов. Изотопы водорода 1Н — протий, 2Н— дейтерий, 3Н — тритий столь сильно отличаются по массе, что и их физические и химические свойства различны. Дейтерий стабилен (т. е. не радиоактивен) и входит в качестве небольшой примеси (1 : 4500) в обычный водород. При соединении дейтерия с кислородом образуется тяжелая вода. Она при нормальном атмосферном давлении кипит при 101,2 °С и замерзает при +3,8 °С. Тритий β-радиоактивен с периодом полураспада около 12 лет.
У всех химических элементов имеются изотопы. У некоторых элементов имеются только нестабильные (радиоактивные) изотопы. Для всех элементов искусственно получены радиоактивные изотопы.
Изотопы урана. У элемента урана есть два изотопа — с массовыми числами 235 и 238. Изотоп![]() составляет всего 1/140 часть от более распространенного
составляет всего 1/140 часть от более распространенного ![]() .
.