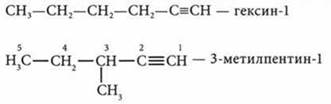Химия - учебно-практический справочник
Алкины - Углеводороды - Органическая химия
Строение. Изомерия. Номенклатура
|
Алкины |
Общая формула СnН2n-2 |
|
Валентный угол: 180° |
|
|
Тип гибридизации атомных орбиталей углерода, соединенных тройной связью: sp |
|
|
Химические связи: наличие одной σ-связи и двух π-связей |
|
|
Длины связей: С≡С составляет 0,120 нм |
|
|
Энергия связей: C≡С составляет 812 кДж/моль |
|
|
Номенклатура: название соответствующего алкана с заменой суффикса -ан на -ин. |
|
Виды изомерии |
Структурная |
Разветвление углеродного скелета |
|
|
Положение тройной связи |
|
||
|
Межклассовая |
Алкины изомерны диенам |
||
Получение алкинов
1. Карбидный метод: ![]()
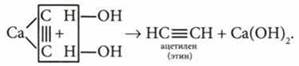
2. Из метана:
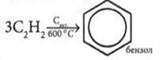
а) пиролиз: ![]()
б) окислительный пиролиз метана: ![]()
3. Взаимодействие дигалогеналкинов соответствующего строения со спиртовым раствором щелочи:

Химические свойства алкинов
|
Реакции соединения (присоединения к Н—С≡С—Н) |
|
|
водорода (kt — Рt, t)
|
Гидрирование (гидрогенизация) |
|
галогенов (Вr2, Сl2)
|
Галогенирование |
|
воды (Hg2+, H+)
|
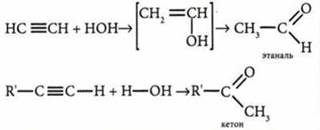
Гидратация (реакция Кучерова). Происходит по правилу Марковникова |
|
Замещение Н возле тройной связи |
|
|
с активными металлами
|
Образуются солеподобные металлические производные ацетиленов |
|
с солями меди(I)
|
Красно-коричневый осадок ацетиленида меди(I) |
|
с солями серебра
|
Белый осадок ацетиленида серебра |
|
Полимеризация |
|
|
циклическая |
Тримеризация |
|
|
|
|
линейная
|
Димеризация |
|
Окисление |
|
|
полное окисление (горение)
|
Горит на воздухе коптящим пламенем |
|
частичное окисление
|
Водный раствор КМnO4 постепенно обесцвечивается |
|
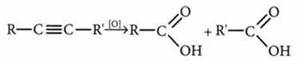
окисление сильными окислителями в кислой среде
|
Окислители: КМnO4, К2Сr2O7 (в кислой среде, озон) |
Качественные реакции на ацетилен (зтин)
1. Взаимодействие с бромной водой:

Бромная вода обесцвечивается.
2. Взаимодействие с аммиачным раствором оксида серебра(I):
![]()
3. Взаимодействие с водным раствором перманганата калия:
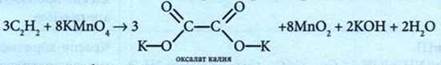
Происходит обесцвечивание раствора.
Алкины определяют с помощью бромной воды (обесцвечивание раствора) и аммиачного раствора оксида серебра(I) (образуется белый осадок).
Ацетилен применяют
1) в производстве каучуков;
2) в производстве синтетических волокон;
3) в производстве уксусной кислоты;
4) в производстве растворителей;
5) при сварке и резке металлов;
6) при получении винилхлорида:
![]()
и поливинилхлорида:

7) при получении уксусного альдегида (этаналя):

ПРОВЕРЬТЕ СЕБЯ
1. Напишите уравнение реакции, схема которой: ![]() Укажите сумму всех коэффициентов.
Укажите сумму всех коэффициентов.
А .
Б .
В .
Г 6
2. Назовите соединения.

3. Получите алкены. Назовите углеводороды, полученные из
А 1-бромбутана
Б 1-иодпропана
В 2-хлор, 2-метилбутана
4. Напишите уравнения реакций, происходящих при взаимодействии 2-метилпентена-2 с
А бромом
Б бромоводородом
В водородом.
5. Напишите уравнения реакций, происходящих при данных преобразованиях.
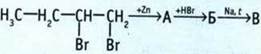
6. С помощью какого реактива можно распознать пробирки с газами этана и этена?
7. Назовите алкины. Укажите тип гибридизации и валентные углы для каждого атома углерода.
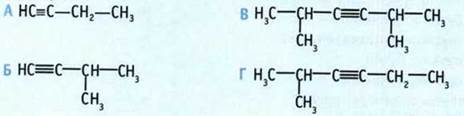
8. Запишите структурные формулы алкинов.
А 3,4-диметилпентин-1
Б 3-этилпентин-1
В 4,4-диметил,3,3-диэтилгептин-1
9. Предложите способы получения
А бутина-2 из н-бутана
Б гексина-3 из метана
10. Напишите уравнения реакций, по которым можно осуществить такие преобразования: ![]()
11. Напишите уравнение термического расщепления гексана, если один из продуктов — бутан.
12. Как, имея углерод, водород и бром, получить 1,1,2,2-тетрабромэтан? Напишите уравнения реакций.
13. Напишите уравнения реакций.
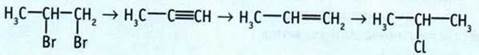
14. Из ацетилена получают поливинилхлорид. Запишите возможные уравнения химических реакций.
ТЕСТОВЫЕ ЗАДАНИЯ
1. Какое вещество относится к ненасыщенным углеводородам?
A С5Н12
Б С3Н8
В С2Н6
Г С2Н4 2. Какой тип реакции характерен для ненасыщенных углеводородов? А замещения Б обмена В соединения Г разложения 3. Изомером бутена-1 является 4. Укажите вещества, которые существуют в виде цис- и транс-изомеров. 5. Веществами-гомологами являются А бутен и пропен Б гексен и 2-метилпентен-1 B бутан и бутен Г пропан и пропен 6. С пропином взаимодействуют А КОН, НСl, КМnO4, Вr2 Б Н2, Вr2, КМnО4, НВr В Вr2, Н2, КСl, Н2O Г ZnBr2, CaO, КМnО4, Н2 7. Укажите правильное утверждение. А Благодаря наличию двух л-связей в молекуле, алкины более реакционноспособны, чем алкены. Б Алкины обесцвечивают бромную воду и водный раствор перманганата калия. В Атом водорода при тройной С—С связи способен замещаться металлом, что указывает на слабые кислотные свойства углерода, который имеет такую группу. Г Ацетилен, вступая в реакции полимеризации, циклополимеризации, образует димер и тример. 8. Веществами-гомологами являются А бутин и этин Б бутин и бутен В пентин и 2-метилбутин-2 Г бутин и бутан 9. Какую массу бромной воды с массовой долей брома 1,6% может обесцветить пропен объемом 1,12 л (н. у.)? А 50 г Б 500 г В 5 г Г 0,5 г 10. Алкен нормального строения имеет двойную связь при первом атоме углерода. Образец этого алкена массой 0,7 л присоединил бром массой 1,6 г. Укажите формулу алкена, назовите его. А С5Н10 Б С6Н12 B С5Н8 Г С7Н]4 11. Алкен массой 4,2 г присоединяет 16 г брома. Найдите молекулярную формулу соединения и укажите ее название. А пропен Б бутен В гексен Г октен 12. Алкен массой 5,6 г присоединил 4,48 л хлороводорода (н. у.). Найдите молекулярную формулу соединения и укажите ее название. А этен Б бутен В пропен Г гексен 13. Алкин массой 6,8 г полностью прореагировал с 32 г брома. Установите молекулярную формулу соединения. А С3Н4 Б С4Н6 B С5Н8 Г С6Н10 14. Укажите молекулярную формулу газообразного углеводорода, если известно, что при сжигании 5,6 л (н. у.) этого вещества образуется 33 г оксида углерода(IV) и 13,5 г воды. А С3Н6 Б С2Н4 В С5Н10 Г С6Н12 15. В результате сжигания углеводорода массой 4,2 г образовался оксид углерода(IV) массой 13,2 г. Относительная плотность пара этого вещества по водороду — 42. Укажите молекулярную формулу углеводорода. А С6Н12 Б С4Н10 В С3Н6 Г С5Н10
![]()

![]()