Химия самостоятельная подготовка к ЕГЭ - универсальные материалы с методическими рекомендациями, решениями и ответами - 2018 год
Биологически важные вещества (жиры, углеводы) - Теоретический материал - ОРГАНИЧЕСКАЯ ХИМИЯ
Жиры
Жиры — сложные эфиры глицерина и высших одноосновных карбоновых кислот.
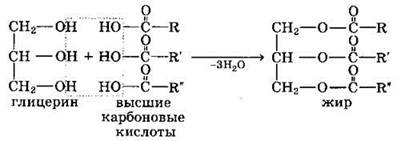
Общее название таких соединений — триглицериды или триацилглицерины, где ацил — остаток карбоновой кислоты C(0)R.
В состав природных триглицеридов входят остатки насыщенных (предельных) кислот (пальмитиновой С15Н31СООН, стеариновой С17Н35СООН и др.) и ненасыщенных (непредельных) кислот (олеиновой С17Н33СООН, линолевой С17Н31СООН, линоленовой С15Н29СООН и др.).
Жиры содержатся во всех растениях и животных. Они представляют собой смеси полных сложных эфиров глицерина и не имеют четко выраженной температуры плавления.
Физические свойства жиров. Животные жиры (бараний, свиной, говяжий и т.п.), как правило, являются твердыми веществами с невысокой температурой плавления (исключение — жидкий рыбий жир).
В твердых жирах преобладают остатки насыщенных кислот.
Растительные жиры — масла (подсолнечное, соевое, хлопковое и др.) — жидкости (исключение — кокосовое масло, масло какао-бобов).
Масла содержат в основном остатки ненасыщенных (непредельных) кислот.
Жидкие жиры превращают в твердые путем реакции гидрогенизации (гидрирования). При этом водород присоединяется по двойной связи, содержащейся в углеводородном радикале молекул масел.
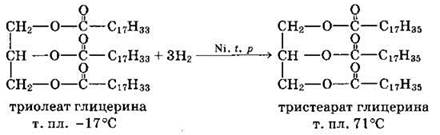
Продукт гидрогенизации масел — твердый жир (искусственное сало, саломас). Маргарин — пищевой жир, состоит из смеси гидрогенизированных масел (подсолнечного, кукурузного, хлопкого и др.), животных жиров, молока и вкусовых добавок (соли, сахара, витаминов и др.).
Жирам как сложным эфирам свойственна обратимая реакция гидролиза, катализируемая минеральными кислотами. При участии щелочей (или карбонатов щелочных металлов) гидролиз жиров происходит необратимо. Продуктами в этом случае являются мыла — соли высших карбоновых кислот и щелочных металлов.
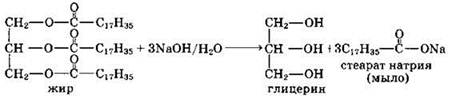
Натриевые соли — твердые мыла, калиевые — жидкие. Реакция щелочного гидролиза жиров, и вообще всех сложных эфиров, называется также омылением.
Жиры, содержащие остатки ненасыщенных кислот, способны к окислению по связям С=С.
Углеводы
Углеводы (сахара) — органические соединения, имеющие сходное строение и свойства, состав большинства которых отражает формула Сx(Н2О)y, где х, у ≥ 3.
Общеизвестные представители: глюкоза, или виноградный сахар, С6Н12O6, сахароза, или тростниковый, свекловичный сахар, С12Н22О11, крахмал и целлюлоза [С6Н10О5]n.
Химические свойства моносахаридов обусловлены наличием в молекуле функциональных групп двух видов: гидроксильных и карбонильных.
Например, глюкоза как многоатомный спирт образует простые и сложные эфиры, комплексное соединение с гидроксидом меди(II) (в щелочной среде).
Как альдегид она окисляется аммиачным раствором оксида серебра, гидроксидом меди(II) и водородом:
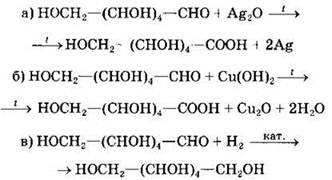
В полуацетальной форме глюкоза способна к нуклеофильному замещению полуацетального гидроксила на группу —OR (образование гликозидов, олиго- и полисахаридов).
Аналогично ведут себя в таких реакциях и другие моносахариды. Важнейшим свойством моносахаридов является их ферментативное брожение, т.е. распад молекул на осколки под действием различных ферментов. Брожению подвергаются в основном гексозы в присутствии ферментов, выделяемых дрожжевыми грибками, бактериями или плесневыми грибками. В зависимости от природы действующего фермента различают реакции следующих видов:
а) спиртовое брожение
![]()
б) молочно-кислое брожение
![]()
в) масляно-кислое брожение
![]()
В живом организме в процессе метаболизма глюкоза окисляется с выделением большого количества энергии:
![]()
Дисахариды — это углеводы, молекулы которых состоят из двух остатков моносахаридов, соединенных друг с другом за счет взаимодействия гидроксильных групп (двух полуацетальных или одной полуацетальной и одной спиртовой). Связи, соединяющие моносахаридные остатки, называются гликозидными.
Примером наиболее распространенных в природе дисахаридов является сахароза. Молекула сахарозы состоит из остатков глюкозы и фруктозы, соединенных друг с другом за счет взаимодействия полуацетальных гидроксилов (1→2)-гликозидной связью:

Физические свойства. Сахароза — бесцветное кристаллическое вещество, очень хорошо растворимое в воде, сладкое на вкус.
Сахароза, находясь в растворе, не вступает в реакцию “серебряного зеркала”, так как не способна превращаться в открытую форму, содержащую альдегидную группу. Подобные дисахариды не способны окисляться (т.е. быть восстановителями) и называются невосстанавливающими сахарами.
Существуют дисахариды, в молекулах которых имеется свободный полуацетальный гидроксил, в водных растворах таких сахаров существует равновесие между открытой и циклической формами молекул. Эти дисахариды легко окисляются, т.е. являются восстанавливающими, например, мальтоза. В мальтозе остатки глюкозы соединены (1→4)-гликозидной связью.

Для дисахаридов характерна реакция гидролиза (в кислой среде или под действием ферментов), в результате которой образуются моносахариды:
![]()
При гидролизе различные дисахариды расщепляются на составляющие их моносахариды за счет разрыва гликозидных связей между ними:
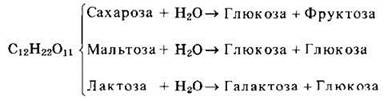
Таким образом, реакция гидролиза дисахаридов является обратной процессу их образования из моносахаридов.
Являясь многоатомным спиртом, сахароза дает синее окрашивание раствора при реакции с Сu(ОН)2.
Полисахариды
Целлюлоза — полимер (С6Н10О5)n с элементарным звеном, представляющим собой остаток β-глюкозы
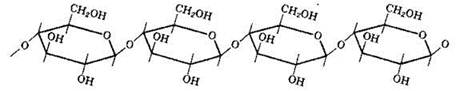
Молекулы целлюлозы имеют линейное строение и большую молекулярную массу. Между молекулами существуют прочные водородные связи. Целлюлоза нерастворима в воде и других растворителях.
Крахмал — полимер такого же состава, что и целлюлоза, но с элементарным звеном, представляющим собой остаток α-глюкозы
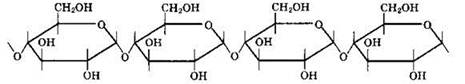
Молекулы крахмала свернуты в спираль, большая часть молекул разветвлена. Молекулярная масса крахмала меньше молекулярной массы целлюлозы. Крахмал — аморфное вещество, нерастворимое в холодной воде, но частично растворимое в горячей.
Химические свойства крахмала и целлюлозы
1. Горение (практическое значение имеет для целлюлозы):
![]()
2. Гидролиз:
![]()
При гидролизе крахмала образуется α-глюкоза, а при гидролизе целлюлозы — β-глюкоза.
3. Качественная реакция на крахмал: с йодом возникает синее окрашивание.
4. Термическое разложение целлюлозы без доступа воздуха приводит к образованию метанола, уксусной кислоты, ацетона и др. продуктов.
С уксусной и азотной кислотой целлюлоза образует сложные эфиры [C6H7O2(ONO2)3]n и [С6Н7O2(OСOСН3)3]n.