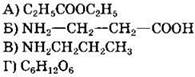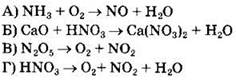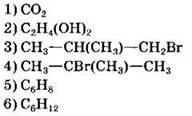Химия самостоятельная подготовка к ЕГЭ - универсальные материалы с методическими рекомендациями, решениями и ответами - 2018 год
ВАРИАНТ 5 - ПРИМЕРНЫЕ ВАРИАНТЫ ЕГЭ
Часть 1
Ответами к заданиям 1—23 является последовательность цифр. Запишите ответ в поле ответа в тексте работы, а затем перенесите в БЛАНК ОТВЕТОВ № 1 справа от номера соответствующего задания, начиная с первой клеточки. Последовательность цифр записывайте без пробелов, запятых и других дополнительных символов. Каждый символ пишите в отдельной клеточке в соответствии с приведенными в бланке образцами.
1. Электронную конфигурацию 1s22s22p6 имеют частицы
1) F
2) O2-
3) S2-
4) Аr
5) Na+
Ответ: ![]()
2. Одинаковую электронную конфигурацию имеют частицы

Ответ: ![]()
3. Ковалентные полярные связи присутствуют в
1) нитрате натрия
2) водороде
3) сероводороде
4) белом фосфоре
5) красном фосфоре
Ответ: ![]()
4. Постоянную степень окисления проявляет:
1) Н и Р
2) О и Na
3) P и N
4) Na и F
5) Sr и Zn
Ответ: ![]()
5. Ионное строение имеет каждое из двух веществ:

Ответ: ![]()
6. Выберите формулы трех несолеобразующих оксидов и запишите соответствующие им номера в ячейки ответа
1) ВеО
2) NO
3) N2O3
4) Аl2O3
5) СО
6) N2O
Ответ: ![]()
7.Сера реагирует с каждым из двух веществ:
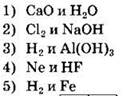
Ответ: ![]()
8. Сернистый газ реагирует с:
1) СаО .
2) NaOH .
3) Н2
4) HF
5) НСl
Ответ: ![]()
9. Гидроксид хрома(III) реагирует с каждым из двух веществ:
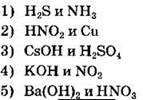
Ответ: ![]()
10. Для перевода пищевой соды в карбонат натрия необходимо
1) прокалить соду
2) добавить гидросульфат калия
3) добавить гидроксид натрия
3) добавить соляную кислоту
4) растворить соду в воде
Ответ: ![]()
11. В заданной схеме превращений
![]()
веществами X и Y являются:
1) Аl2O3
2) Аl(ОН)3
3) NaOH (в растворе)
4) NaOH (при сплавлении)
5) Na2CO3 (в растворе)
Ответ: ![]()
12. Число σ- и π-связей в молекуле пропина равно
1) 1
2) 2
3) 3
4) 4
5) 6
Ответ: 
13. Пентин-1, в отличие от пентана, реагирует с
1) бромом
2) бромной водой
3) аммиачным раствором оксида серебра
4) кислородом
5) пропаном
Ответ: ![]()
14. Глицерин реагирует с
1) оксидом железа(III)
2) гидроксидом меди(II)
3) перманганатом калия
4) пропаном
5) оксидом углерода(IV)
Ответ: ![]()
15. Фенол реагирует с
1) бутаном
2) пропилацетатом
3) бромом
4) водородом
5) гидрокарбонатом натрия
Ответ: ![]()
16. Этаналь можно получить при действии на этан
1) оксида меди(II)
2) серной кислоты
3) перманганата калия
4) бромной воды
5) этиленгликоля
Ответ: ![]()
17. Метиламин — более сильное основание, чем
1) диметиламин
2) анилин
3) триметиламин
4) аммиак
5) гидроксид натрия
Ответ: ![]()
18. В заданной схеме превращений
![]()
веществами X и Y являются:
1) карбид кальция
2) оксид азота(V)
3) карбид алюминия
4) нитрат натрия
5) азотная кислота
Ответ: ![]()
19. Из предложенного перечня выберите две характеристики реакции взаимодействия этанола с уксусной кислотой.
1) каталитическая
2) обратимая
3) эндотермическая
4) окислительно-восстановительная
5) присоединения
Ответ: ![]()
20. Для уменьшения скорости реакции ![]() следует
следует
1) измельчить железо
2) увеличить концентрацию FeCl2
3) добавить катализатор
4) уменьшить концентрацию кислоты
5) понизить температуру
Ответ: ![]()
21. Сокращенное ионное уравнение ![]() соответствует растворению гидроксида железа в кислоте
соответствует растворению гидроксида железа в кислоте
1) соляной
2) плавиковой
3) уксусной
4) сероводородной
5) азотной
Ответ: ![]()
22. Растворы глюкозы и фруктозы можно различить с помощью
1) водного раствора КОН
2) аммиачного раствора оксида серебра
3) раствора серной кислоты
4) гидроксида алюминия
5) гидроксида меди(II)
Ответ: ![]()
23. Колонна синтеза используется в процессе получения
1) аммиака
2) сернистого газа
3) газойля из нефти
4) железа из руды
5) метанола
Ответ: ![]()
Ответом к заданиям 24-26 является число. Запишите это число в поле ответа в тексте работы, соблюдая при этом указанную степень точности. Затем перенесите это число в БЛАНК ОТВЕТОВ № 1 справа от номера соответствующего задания, начиная с первой клеточки. Каждый символ пишите в отдельной клеточке в соответствии с приведенными в бланке образцами. Единицы измерения физических величин писать не нужно.__
24. Рассчитайте, сколько граммов нитрата калия следует растворить в 50 г 5%-ного раствора соли для получения 8%-ного раствора?
Ответ: ____ г (запишите число с точностью до десятых).
25. В соответствии с термохимическим уравнением ![]() окисление 11 л (н.у.) сернистого газа сопровождается выделением ______ кДж теплоты. (Запишите ответ с точностью до целых).
окисление 11 л (н.у.) сернистого газа сопровождается выделением ______ кДж теплоты. (Запишите ответ с точностью до целых).
26. Вычислите массу оксида серы(IV), образующегося при обжиге 9,6 г сульфида меди(II).
Ответ: _____ г (запишите число с точностью до десятых).
В заданиях 27—35 к каждому элементу первого столбца подберите соответствующий элемент из второго столбца и запишите в таблицу выбранные цифры под соответствующими буквами. Получившуюся последовательность цифр перенесите в БЛАНК ОТВЕТОВ № 1 без пробелов, запятых и других дополнительных символов. Цифры в ответе могут повторяться..
27. Установите соответствие между формулой соединения и классом, к которому это вещество принадлежит.
|
ФОРМУЛА СОЕДИНЕНИЯ
|
КЛАСС/ГРУППА 1) амины 2) аминокислоты 3) простые эфиры 4) сложные эфиры 5) дипептиды 6) углеводы |
Ответ: 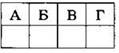
28. Установите соответствие между схемой реакции и свойством азота, которое этот элемент проявляет в данной реакции.
|
СХЕМА РЕАКЦИИ
|
СВОЙСТВО АЗОТА 1) только окислитель 2) только восстановитель 3) и окислитель, и восстановитель 4) ни окислитель, ни восстановитель |
Ответ: 
29. Установите соответствие между формулой соли и продуктом, выделяющимся на аноде в ходе электролиза водного раствора этой соли.
|
ФОРМУЛА СОЛИ
|
ПРОДУКТ НА АНОДЕ 1) фтор 2) бром 3) иод 4) медь 5) кислород 6) сера |
Ответ: 
30. Установите соответствие между формулой соли и средой ее водного раствора.
|
ФОРМУЛА СОЛИ
|
СРЕДА РАСТВОРА 1) нейтральная 2) кислая 3) щелочная |
Ответ: 
31. Установите соответствие между способом воздействия на равновесную систему
![]()
и направлением смещения химического равновесия в результате этого воздействия:
|
ВОЗДЕЙСТВИЕ НА СИСТЕМУ A) уменьшение давления Б) добавление катализатора B) увеличение температуры Г) увеличение концентрации хлора |
НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ 1) в сторону продуктов реакции 2) в сторону исходных веществ 3) практически не смещается |
Ответ: 
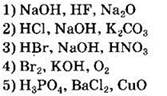
32. Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может реагировать.
|
ФОРМУЛА ВЕЩЕСТВА
|
РЕАГЕНТЫ
|
Ответ: 
33. Установите соответствие между формулами взаимодействующих веществ и признаком химической реакции, протекающей между ними.
|
ФОРМУЛЫ ВЕЩЕСТВ A) гексен-2 и Вr2 (водн.) Б) бутин-1 и КМnO4 (Н+) B) уксусная кислота и КОН Г) уксусная кислота и FeO |
ПРИЗНАК РЕАКЦИИ 1) выделение газа 2) обесцвечивание раствора 3) образование осадка 4) растворение осадка 5) видимые признаки реакции отсутствуют |
Ответ: 
34. Установите соответствие между схемой реакции и формулой органического продукта, преимущественно образующегося в ходе реакции.
|
СХЕМА РЕАКЦИИ
|
ФОРМУЛА ПРОДУКТА
|
Ответ: 
35. Установите соответствие между схемой реакции и названием органического продукта, преимущественно образующегося в ходе реакции.
|
СХЕМА РЕАКЦИИ
|
НАЗВАНИЕ ПРОДУКТА 1) метан 2) пропановая кислота 3) этановая кислота 4) угарный газ 5) углекислый газ 6) водород |
Ответ: 
Часть 2
Для записи ответов на задания 36-40 используйте БЛАНК ОТВЕТОВ № 2. Запишите сначала номер задания (36, 37 и т.д.), а затем его подробное решение. Ответы записывайте четко и разборчиво.
36. Используя метод электронного баланса, составьте уравнение реакции
![]()
Определите окислитель и восстановитель.
37. Алюминий прореагировал с бромом. Продукт растворили в воде и обработали раствором пищевой соды. Выпавший осадок растворили в иодоводородной кислоте. Полученную соль обработали перманганатом калия в сернокислой среде. Напишите уравнения четырех описанных реакций.
38. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
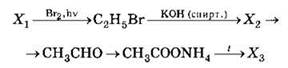
При написании уравнений реакций используйте структурные формулы органических веществ.
39. Смесь гидросульфата и сульфата натрия с массовой долей сульфата в ней 60% может прореагировать с 144 мл 10%-ного раствора гидроксида натрия (ρ = 1,11 г/мл). На исходную смесь подействовали избытком раствора гидроксида бария. Найдите массу осадка, образовавшегося при этом.
40. В результате реакции предельного двухатомного спирта массой 30,4 г с избытком металлического натрия получено 8,96 л (н.у.) газа. Указанный спирт не взаимодействует со свежеполученным осадком гидроксида меди(П). На основании этих данных:
1) произведите вычисления, необходимые для установления молекулярной формулы спирта;
2) запишите молекулярную формулу спирта;
3) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле;
4) приведите уравнение реакции его взаимодействия с металлическим натрием.