Химия 9 класс - поурочные разработки
Понятие о скорости химической реакции. Катализаторы. Химическое равновесие
Цели урока: повторить и закрепить знания об обратимых реакциях, химическом равновесии; сформировать представления о катализаторах и катализе.
Ход урока
1. Организационный момент урока.
2. Изучение нового материала.
Вы знакомы с понятием "скорость" из курса физики. В общем виде скорость - это величина, показывающая как изменяется какая либо характеристика за единицу времени.
Скорость химической реакции - это величина, показывающая как изменяются концентрации исходных веществ или продуктов реакции за единицу времени.
Для оценки скорости необходимо изменение концентрации одного из веществ.
1. Наибольший интерес представляют реакции, протекающие в однородной (гомогенной) среде.
Гомогенные системы (однородные) – газ/газ, жидкость/жидкость – реакции идут во всём объёме.
Математически скорость химической гомогенной реакции можно представить с помощью формулы.
2. Для гетерогенной реакции, скорость реакции определяется числом молей веществ, вступивших в или образующихся в результате реакции в единицу времени на единице поверхности.
Скорость реакции в гетерогенной среде:
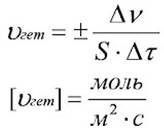
S – площадь поверхности, (м2).
Гетерогенные (неоднородные) системы – твёрдое/жидкость, газ/твёрдое, жидкость/газ – реакции идут на поверхности раздела фаз.
Таким образом, скорость химической реакции показывает изменение количества вещества в единицу времени, в единице объёма или на единице поверхности раздела фаз.
Зависимость скорости реакций от различных факторов:
Условия |
Примеры |
концентрация |
Закон действующих масс Скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ. При повышении концентрации хотя бы одного из реагирующих веществ скорость химической реакции возрастает в соответствии с кинетическим уравнением. aA +bB = cC + dD, где A,B,C,D – газы, жидкости Для данной реакции кинетическое уравнение принимает вид:
Причиной повышения скорости является увеличение числа столкновений реагирующих частиц за счёт увеличения частиц в единице объёма. |
температура |
Химические реакции, протекающие в гомогенных системах (смеси газов, жидкие растворы), осуществляется за счет соударения частиц. Однако, не всякое столкновение частиц реагентов ведет к образованию продуктов. Только частицы, обладающие повышенной энергией - активные частицы, способны осуществить акт химической реакции. С повышением температуры увеличивается кинетическая энергия частиц и число активных частиц возрастает, следовательно, химические реакции при высоких температурах протекают быстрее, чем при низких температурах. Зависимость скорости реакции от температуры определяется правилом Вант - Гоффа: при повышении температуры на каждые 10 °С скорость реакции увеличивается в 2-4 раза.
Правило Вант - Гоффа является приближенным и применимо лишь для ориентировочной оценки влияния температуры на скорость реакции. |
катализатор |
Катализаторы - это вещества, которые повышают скорость химической реакции. Они вступают во взаимодействие с реагентами с образованием промежуточного химического соединения и освобождаются в конце реакции. Влияние, оказываемое катализаторами на химические реакции, называется катализом. По агрегатному состоянию, в котором находятся катализатор и реагирующие вещества, следует различать: гомогенный катализ (катализатор образует с реагирующими веществами гомогенную систему, например, газовую смесь); гетерогенный катализ (катализатор и реагирующие вещества находятся в разных фазах; катализ идет на поверхности раздела фаз). Ингибитор - вещество, замедляющее скорость реакции. |
площадь соприкосновения реагирующих веществ |
Для увеличения площади соприкосновения реагирующих веществ, их измельчают. Наибольшей степени измельчения достигают путем растворения веществ. Быстрее всего вещества реагируют в растворах. |
природа реагирующих веществ |
Например, металлы магний и железо реагируют с соляной кислотой одинаковой концентрации с различной скоростью. Это связано с разной химической активностью металлов. |
1. Среди всех известных реакций различают реакции обратимые и необратимые. При изучении реакций ионного обмена были перечислены условия, при которых они протекают до конца. (вспомните их).
Известны и такие реакции, которые при данных условиях до конца не идут. Так, например, при растворении в воде сернистого газа происходит реакция: SO2 + H2O → H2SO3. Но оказывается, что в водном растворе может образоваться только определенное количество сернистой кислоты. Это объясняется тем, что сернистая кислота непрочная, и происходит обратная реакция, т.е. разложение на оксид серы и воду. Следовательно, данная реакция не идет до конца потому, что одновременно происходит две реакции – прямая (между оксидом серы и водой) и обратная(разложение сернистой кислоты). SO2 + H2O ↔ H2SO3.
Химические реакции, протекающие при данных условиях во взаимно противоположных направлениях, называются обратимыми.
2. Поскольку скорость химических реакций зависит от концентрации реагирующих веществ, то вначале скорость прямой реакции (υпр) должна быть максимальной, а скорость обратной реакции (υобр) равняется нулю. Концентрация реагирующих веществ с течением времени уменьшается, а концентрация продуктов реакции увеличивается. Поэтому скорость прямой реакции уменьшается, а скорость обратной реакции увеличивается. В определенный момент времени скорость прямой и обратной реакций становятся равными:

Во всех обратимых реакциях скорость прямой реакции уменьшается, скорость обратной реакции возрастает до тех пор, пока обе скорости не станут равными и не установится состояние равновесия:
υпр = υобр
Состояние системы, при котором скорость прямой реакции равна скорости обратной реакции, называют химическим равновесием.
В состоянии химического равновесия количественное соотношение между реагирующими веществами и продуктами реакции остается постоянным: сколько молекул продукта реакции в единицу времени образуется, столько их и разлагается. Однако состояние химического равновесия сохраняется до тех пор, пока остаются неизменными условия реакции: концентрация, температура и давление.
Количественно состояние химического равновесия описывается законом действующих масс.
При равновесии отношение произведения концентраций продуктов реакции (в степенях их коэффициентов) к произведению концентраций реагентов (тоже в степенях их коэффициентов) есть величина постоянная, не зависящая от исходных концентраций веществ в реакционной смеси.
Эта постоянная величина называется константой равновесия – k.
Так для реакции: N2 (Г) + 3H2 (Г) ↔ 2NH3 (Г) + 92,4 кДж константа равновесия выражается так:
υ1 = υ2
υ1 (прямой реакции) = k1[N2][H2]3 , где [] – равновесные молярные концентрации, [] = моль/л,
υ2 (обратной реакции) = k2 [NH3]2
k1[N2][H2]3 = k2 [NH3]2
Kp = k1/k2 = [NH3]2/ [N2][H2]3 – константа равновесия.
Химическое равновесие зависит – от концентрации, давления, температуры.
Принцип Ле-Шателье определяет направление смешения равновесия:
Если на систему, находящуюся в равновесии оказали внешнее воздействие, то равновесие в системе сместится в сторону обратную этому воздействию.
1) Влияние концентрации – если увеличить концентрацию исходных веществ, то равновесие смещается в сторону образования продуктов реакции.
Например, Kp = k1/k2 = [NH3]2/ [N2][H2]3
При добавлении в реакционную смесь, например азота, т.е. возрастает концентрация реагента, знаменатель в выражении для К увеличивается, но так как К – константа, то для выполнения этого условия должен увеличиться и числитель. Таким образом, в реакционной смеси возрастает количество продукта реакции. В таком случае говорят о смещении химического равновесия вправо, в сторону продукта.
Таким образом, увеличение концентрации реагентов (жидких или газообразных) смещает в сторону продуктов, т.е. в сторону прямой реакции. Увеличение концентрации продуктов (жидких или газообразных) смещает равновесие в сторону реагентов, т. е. в сторону обратной реакции.
Изменение массы твердого вещества не изменяет положение равновесия.
2) Влияние температуры – увеличение температуры смещает равновесие в сторону эндотермической реакции.
а) N2 (Г) + 3H2 (Г) ↔ 2NH3 (Г) + 92,4 кДж (экзотермическая – выделение тепла)
При повышении температуры равновесие сместится в сторону реакции разложения аммиака (←)
б) N2 (Г) + O2 (Г) ↔ 2NO (Г) – 180,8 кДж (эндотермическая - поглощение тепла)
При повышении температуры равновесие сместится в сторону реакции образования NO (→)
3) Влияние давления (только для газообразных веществ) – при увеличении давления, равновесие смещается в сторону образования веществ, занимающих меньший объём.
N2 (Г) + 3H2 (Г) ↔ 2NH3 (Г)
1V - N2
3V - H2
2V – NH3
При повышении давления (P): до реакции 4V газообразных веществ → после реакции 2V газообразных веществ, следовательно, равновесие смещается вправо (→)
При увеличении давления, например, в 2 раза, объём газов уменьшается в такое же количество раз, а следовательно, концентрации всех газообразных веществ возрастут в 2 раза. Kp = k1/k2 = [NH3]2/ [N2][H2]3
В этом случае числитель выражения для К увеличится в 4 раза, а знаменатель в 16 раз, т.е. равенство нарушится. Для его восстановления должны возрасти концентрация аммиака и уменьшиться концентрации азота и водорода. Равновесие сместится вправо.
Итак, при повышении давления равновесие смещается в сторону уменьшения объема, при понижении давления – в сторону увеличения объёма.
Изменение давления практически не сказывается на объёме твердых и жидких веществ, т.е. не изменяет их концентрацию. Следовательно, равновесие реакций, в которых газы не участвуют, практически не зависит от давления.
! На течение химической реакции влияют вещества – катализаторы. Но при использовании катализатора понижается энергия активации как прямой, так и обратной реакции на одну и ту же величину и поэтому равновесие не смещается.
3. Закрепление изученного материала
Задача
Укажите, как повлияет:
а) повышение давления;
б) повышение температуры;
в) увеличение концентрации кислорода на равновесие системы:
2CO (г) + O2 (г) ↔ 2CO2 (г) + Q
Решение:
а) Изменение давления смещает равновесие реакций с участием газообразных веществ (г). Определим объёмы газообразных веществ до и после реакции по стехиометрическим коэффициентам:
По принципу Ле-Шателье, при увеличении давления, равновесие смещается в сторону образования веществ, занимающих меньший объём, следовательно равновесие сместится вправо, т. е. в сторону образования СО2, в сторону прямой реакции (→).
б) По принципу Ле-Шателье, при повышении температуры, равновесие смещается в сторону эндотермической реакции (-Q), т.е. в сторону обратной реакции – реакции разложения СО2 (←), т.к. по закону сохранения энергии:
Q - 2CO (г) + O2 (г) ↔ 2CO2 (г) + Q
в) При увеличении концентрации кислорода равновесие системы смещается в сторону получения СО2 (→) т. к. увеличение концентрации реагентов (жидких или газообразных) смещает в сторону продуктов, т.е. в сторону прямой реакции.
4. Домашнее задание.
П. 14.
Выполнить задание по парам.
Пример 1. Во сколько раз изменится скорость прямой и обратной реакции в системе:
2SO2(г) + O2(г) = 2SO3(г)
если объем газовой смеси уменьшить в три раза? В какую сторону сместится равновесие системы?
Решение. Обозначим концентрации реагирующих веществ: [SO2]= a, [О2] = b,[SO3] = с. Согласно закону действия масс скорости v прямой и обратной реакции до изменения объема:
vпр = Ка2b
vобр = К1с2.
После уменьшения объема гомогенной системы в три раза концентрация каждого из реагирующих веществ увеличится в три раза: [SO2] = 3а, [О2] = 3b; [SO3] = 3с. При новых концентрациях скорости v’ прямой и обратной реакции:
v’пр = К(3а)2(3b) = 27Ка2b
v’обр = К1(3с)2 = 9К1с2
Отсюда:
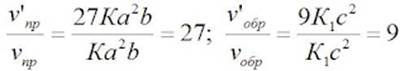
Следовательно, скорость прямой реакции увеличилась в 27 раз, а обратной – только в девять раз. Равновесие системы сместилось в сторону образования SO3.
Пример 2. Вычислите, во сколько раз увеличится скорость реакции, протекающей в газовой фазе, при повышении температуры от 30 до 70 °С, если температурный коэффициент реакции равен 2.
Решение. Зависимость скорости химической реакции от температуры определяется эмпирическим правилом Вант-Гоффа по формуле:

Следовательно, скорость реакции νТ2 при температуре 70 °С больше скорости реакции νТ1 при температуре 30 °С в 16 раз.
Пример 3. Константа равновесия гомогенной системы:
СО(г) + Н2О(г) = СО2(г) + Н2(г)
при 850 °С равна 1. Вычислите концентрации всех веществ при равновесии, если исходные концентрации: [СО]исх =3 моль/л, [Н2О]исх = 2 моль/л.
Решение. При равновесии скорости прямой и обратной реакций равны, а отношение констант этих скоростей постоянно и называется константой равновесия данной системы:
vпр = К1 [СО][Н2О]
vобр = К2[СО2][Н2]
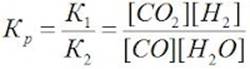
В условии задачи даны исходные концентрации, тогда как в выражение Крвходят только равновесные концентрации всех веществ системы. Предположим, что к моменту равновесия концентрации [СО2]р = х моль/л. Согласно уравнению системы число молей образовавшегося водорода при этом будет также х моль/л. По столько же молей (х моль/л) СО и Н2О расходуется для образования по х молей СО2 и Н2. Следовательно, равновесные концентрации всех четырех веществ:
[СО2]р = [Н2]р = х моль/л;
[СО]р = (3 – х) моль/л;
[Н2О]р = (2 – х) моль/л.
Зная константу равновесия, находим значение х, а затем исходные концентрации всех веществ:
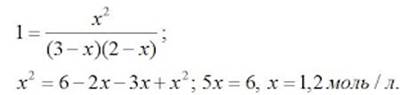
Таким образом, искомые равновесные концентрации:
[СО2]р = 1,2 моль/л;
[Н2]р= 1,2 моль/л;
[СО]р = 3 – 1,2 = 1,8 моль/л;
[Н2О]р = 2 – 1,2 = 0,8 моль/л.

